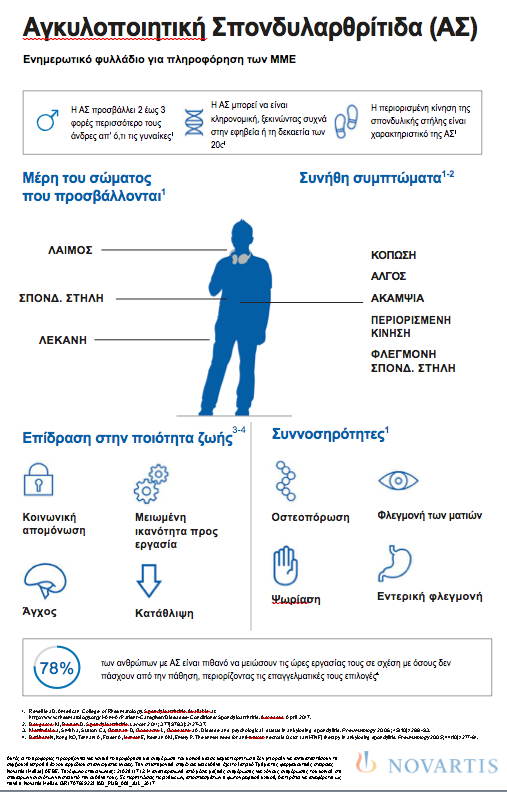
Η αγκυλοποιητική σπονδυλαρθρίτιδα (ΑΣ) ανήκει στην οικογένεια των χρόνιων φλεγμονωδών νόσων που περιλαμβάνει και την ΨΑ. Γενικά, οδηγεί σε σοβαρή υποβάθμιση της κινητικότητας της σπονδυλικής στήλης και της σωματικής λειτουργίας, η οποία έχει αντίκτυπο στην ποιότητα ζωής. Συνήθως, προσβάλλει κυρίως άνδρες κατά τη διάρκεια της εφηβείας και κατά τη δεύτερη δεκαετία της ζωής τους. Τα μέλη της οικογένειας των ασθενών με ΑΣ διατρέχουν υψηλότερο κίνδυνο.
Η ΑΣ είναι μια χρόνια, φλεγμονώδης νόσος που προκαλεί πόνο και ακαμψία στη σπονδυλική στήλη και στις αρθρώσεις και μπορεί να οδηγήσει σε σημαντική απώλεια κινητικότητας, εάν δεν αντιμετωπιστεί καταλλήλως. Πολλοί ασθενείς με ΑΣ ανταποκρίνονται ανεπαρκώς στις θεραπείες με αντι-TNF παράγοντες που αποτελούν την τρέχουσα θεραπεία εκλογής. Σε σοβαρές περιπτώσεις, μπορεί να παρατηρηθεί η σπονδυλική σύντηξη της σπονδυλικής στήλης και των αρθρώσεων επάνω από τον κόκκυγα. Απαιτείται ακτινογραφία, αξονική τομογραφία (CT) ή μαγνητική απεικόνιση (MRI) της σπονδυλικής στήλης ή των ιερολαγόνιων αρθρώσεων για την παρακολούθηση της εξέλιξης της ΑΣ και της αποτελεσματικότητας της θεραπείας.
Οι βελτιώσεις στα συμπτώματα της ΑΣ μετριούνται με τα κριτήρια ανταπόκρισης ASAS (ASAS 20), τα οποία ορίζονται ως βελτίωση κατά τουλάχιστον 20% και απόλυτη βελτίωση κατά τουλάχιστον 10 μονάδες σε κλίμακα 0-100 mm, σε τουλάχιστον τρία από τα παρακάτω κριτήρια: βελτίωση της ευκαμψίας, του πόνου κατά τη διάρκεια της νύχτας, της ικανότητας επιτέλεσης συγκεκριμένων εργασιών, της πρωινής δυσκαμψίας, και απουσία περαιτέρω επιδείνωσης της κατάστασης. Το ποσοστό των ασθενών που πέτυχαν ανταπόκριση ASAS20 είναι ένας αποδεκτός τρόπος μέτρησης της αποτελεσματικότητας των θεραπειών της ΑΣ.
Η Novartis ανακοίνωσε νέα μακροπρόθεσμα δεδομένα για τη χρήση της σεκουκινουμάμπης σε ασθενείς με αγκυλοποιητική σπονδυλαρθρίτιδα (ΑΣ). Αυτή η μελέτη είναι μοναδική, καθώς τα εν λόγω δεδομένα καταδεικνύουν, για πρώτη φορά σε σχέση με οποιονδήποτε βιολογικό παράγοντα, ότι ποσοστό σχεδόν 80% των ασθενών με ΑΣ που έλαβαν θεραπεία με σεκουκινουμάμπη δεν εμφάνισαν ακτινολογική εξέλιξη (mSASSS <2 4=”” span=””>. Τα νέα δεδομένα επιβεβαιώνουν επίσης ότι επιτυγχάνονται διατηρούμενες βελτιώσεις στα σημεία και τα συμπτώματα σε ποσοστό σχεδόν 80% των ασθενών, ενώ η σεκουκινουμάμπη εμφανίζει ευνοϊκό και συνεπές προφίλ ασφαλείας. Τα νέα δεδομένα παρουσιάστηκαν ως σημαντική ανακάλυψη στο ετήσιο συνέδριο για το 2017 του Αμερικανικού Κολεγίου Ρευματολογίας/Συνδέσμου Ρευματολόγων Επαγγελματιών Υγείας (ACR/ARHP), που πραγματοποιήθηκεστο Σαν Ντιέγκο των Ηνωμένων Πολιτειών.
Αυτά τα νέα μακροπρόθεσμα δεδομένα έρχονται να προστεθούν σε έναν αυξανόμενο όγκο στοιχείων που αποδεικνύουν ότι η σεκουκινουμάμπηκατέχει μοναδική θέση στη θεραπεία της ΑΣ, της ψωριασικής αρθρίτιδας (ΨΑ) και της μέτριας έως σοβαρής ψωρίασης, χάρη στη μακροχρόνια αποτελεσματικότητά του και το αποδεδειγμένο προφίλ ασφαλείας του1,3–6. Η σεκουκινουμάμπη είναι ο πρώτος και ο μοναδικός εγκεκριμένος αναστολέας της IL-17A για τη θεραπεία της ΑΣ. Η σεκουκινουμάμπη είναι ένας βιολογικός παράγοντας με ιδιαίτερη στόχευση για χρήση ως θεραπεία της ΑΣ, μια χρόνια φλεγμονώδη νόσο που μπορεί να οδηγήσει σε παρατεταμένο πόνο και απώλεια της κινητικότητας.
«Το κύριο εύρημα που προκύπτει από αυτά τα δεδομένα είναι ότι οι ασθενείς που λαμβάνουν θεραπεία με σεκουκινουμάμπη μπορεί να έχουν πλέον τη δυνατότητα να διατηρήσουν την κινητικότητά τους για μεγαλύτερο χρονικό διάστημα. Αυτό είναι πολύ σημαντικό, καθώς η αγκυλοποιητική σπονδυλαρθρίτιδα είναι μια πάθηση που προκαλεί αναπηρία και μπορεί να προσβάλει έναν άνθρωπο κατά τη δεύτερη δεκαετία της ζωής του, όταν έχει ακόμη πολλά χρόνια να ζήσει», δήλωσε ο Vas Narasimhan, Global Head, DrugDevelopment και Chief Medical Officer της Novartis. «Για πρώτη φορά για οποιονδήποτε βιολογικό παράγοντα, η σεκουκινουμάμπη δείχνει ότι σχεδόν 80% των ασθενών δεν εμφάνισαν ακτινολογική εξέλιξη για διάστημα έως και 4 ετών. Αυτά τα δεδομένα καταδεικνύουν ότι η σεκουκινουμάμπη μπορεί να βοηθήσει τους ασθενείς να ζήσουν με λιγότερο πόνο και να διατηρήσουν την κινητικότητά τους για μεγαλύτερο χρονικό διάστημα».
Σχετικά με την σεκουκινουμάμπη και την IL-17A
Η σεκουκινουμάμπη είναι ο πρώτος και ο μοναδικός πλήρως ανθρώπινος αναστολέας της IL-17A που είναι εγκεκριμένος για τη θεραπεία της ΑΣ, της ΨΑ και της ψωρίασης7. Η σεκουκινουμάμπη είναι μια στοχευμένη θεραπεία που αναστέλλει συγκεκριμένα την κυτταροκίνη IL-17A, η οποία διαδραματίζει σημαντικό ρόλο στην παθογένεση της ΑΣ, της ΨΑ και της ψωρίασης κατά πλάκας. Η σεκουκινουμάμπη είναι ο πρώτος αναστολέας IL-17A που έχει εγκριθεί για τη θεραπεία της ενεργού ΑΣ και της ΨΑ σε περισσότερες από 70 χώρες, μεταξύ των οποίων στις χώρες της Ευρωπαϊκής Ένωσης και στις Ηνωμένες Πολιτείες. Η σεκουκινουμάμπη είναι επίσης εγκεκριμένη για τη θεραπεία της ΨΑ και της φλυκταινώδους ψωρίασης στην Ιαπωνία.
Επιπλέον, η σεκουκινουμάμπη είναι εγκεκριμένη για τη θεραπεία της μέτριας έως σοβαρής ψωρίασης κατά πλάκας σε περισσότερες από 75 χώρες, μεταξύ των οποίων στις χώρες της Ευρωπαϊκής Ένωσης, στην Ιαπωνία, την Ελβετία, την Αυστραλία, τις ΗΠΑ και τον Καναδά. Στην Ευρώπη, η σεκουκινουμάμπηείναι εγκεκριμένη για τη συστημική θεραπεία πρώτης γραμμής της μέτριας έως σοβαρής ψωρίασης κατά πλάκας σε ενήλικες ασθενείς. Στις ΗΠΑ, η σεκουκινουμάμπη είναι εγκεκριμένη ως θεραπεία για τη μέτρια έως σοβαρή ψωρίαση κατά πλάκας σε ενήλικες ασθενείς που είναι υποψήφιοι για συστημική θεραπεία ή φωτοθεραπεία.
Σχετικά με τη μελέτη MEΑSURE 1
Η μελέτη MEASURE 1 είναι μια διετής, πολυκεντρική, τυχαιοποιημένη, ελεγχόμενη με εικονικό φάρμακο μελέτη Φάσης ΙΙΙ για την αξιολόγηση της αποτελεσματικότητας και της ασφάλειας της σεκουκινουμάμπης σε ασθενείς με ενεργή ΑΣ. Συνολικά, 290 από τους 371 ασθενείς ολοκλήρωσαν τη δοκιμή, μετά το πέρας της οποίας 274 ασθενείς κλήθηκαν να συμμετάσχουν σε μια 3ετή περίοδο παράτασης. Τα πρωτεύοντα καταληκτικά σημεία περιελάμβαναν την αξιολόγηση της ανωτερότητας της σεκουκινουμάμπηςέναντι του εικονικού φαρμάκου κατά την Εβδομάδα 16 στο ποσοστό των ασθενών που πέτυχαν βελτίωση τουλάχιστον κατά 30% στην ανταπόκριση κατά ASAS20 (κριτήρια ανταπόκρισης της Διεθνούς Εταιρείας για την Αξιολόγηση της Σπονδυλαρθρίτιδας). Από την Εβδομάδα 16, οι ασθενείς που περιλαμβάνονταν στο σκέλος του εικονικού φαρμάκου επανατυχαιοποιήθηκαν για τη λήψη σεκουκινουμάμπης 75mg ή 150mg, ανάλογα με την ανταπόκριση κατά ASAS. Οι μη ανταποκρινόμενοι ασθενείς άλλαξαν θεραπεία κατά την Εβδομάδα 16 και οι ανταποκρινόμενοι ασθενείς κατά την Εβδομάδα 24.
Από τους ασθενείς που συμμετείχαν στη μελέτη, ποσοστό σχεδόν 80% δεν εμφάνισαν ακτινολογική εξέλιξη σε διάστημα 208 εβδομάδων θεραπείας, όπως αποδεικνύεται από την αξιολόγηση των ακτινογραφιών μέσω της τροποποιημένης Βαθμολογίας Σπονδυλικής Στήλης ΑγκυλοποιητικήςΣπονδυλαρθρίτιδας του Stoke (mSΑSSS). Το σημαντικότερο είναι ότι η μηεξέλιξη της δομικής βλάβης της ΑΣ στη σπονδυλική στήλη συσχετίστηκε με τα διατηρούμενα αποτελέσματα στις μετρήσεις του πόνου που αναφέρεται από τον ασθενή, ενώ σε ποσοστό άνω του 75% των ασθενών η ανταπόκριση ASAS20 διατηρήθηκε για διάστημα 4 ετών. Το προφίλ ασφαλείας της σεκουκινουμάμπης φάνηκε να συνάδει με εκείνο που παρατηρήθηκε σε κλινικές δοκιμές για πολλαπλές ενδείξεις.
Πηγή: http://medlabgr.blogspot.com
 Ιατρικά Νέα Θέματα για την υγεία | Το εγκυρότερο ελληνικό portal με θέματα υγείας, διατροφής, ομορφιάς, φυσικής κατάστασης, ιατρικών θεμάτων
Ιατρικά Νέα Θέματα για την υγεία | Το εγκυρότερο ελληνικό portal με θέματα υγείας, διατροφής, ομορφιάς, φυσικής κατάστασης, ιατρικών θεμάτων